Os lipopolissacarídeos (LPS) são endotoxinas bacterianas formadas a partir de fosfolipídeos da parede celular de gram-negativas, liberados quando há destruição dessas células. Sua dosagem pode ser utilizada para avaliar a função do sistema imunológico , bem como os níveis inflamatórios decorrentes da infecção. A presença de LPS indica a presença de uma infecção por essas bactérias, auxiliando no diagnóstico de doenças como sepse, pneumonia e meningite. Além disso, o LPS é um potente indutor da resposta inflamatória inata, ativando células imunes.
Aplicações clínicas:
· Diagnóstico e Prognóstico de Sepse: A sepse é uma condição com risco de vida causada por uma resposta imunológica desregulada à infecção. A dosagem sérica de LPS pode auxiliar no diagnóstico e prognóstico da sepse. Níveis elevados de LPS na corrente sanguínea indicam a presença de infecção bacteriana gram-negativa, que é uma causa comum de sepse.
· Monitoramento de infecções bacterianas: A medição sérica de LPS pode ser usada para monitorar a eficácia da terapia antibiótica em infecções bacterianas. Pode ajudar a avaliar a resposta ao tratamento, acompanhando a redução nos níveis de LPS ao longo do tempo. A elevação persistente de LPS pode indicar falha do tratamento ou a presença de bactérias resistentes a antibióticos.
· Síndrome do Intestino Irritável (SII) : pode ser usado também como um biomarcador do nível de inflamação em pacientes com Síndrome do Intestino Irritável (SII), uma vez que altos níveis de LPS estão relacionados com aumento da permeabilidade intestinal (leaky gut).
· Disbiose Intestinal : a dosagem de LPS pode fornecer informações sobre a translocação de endotoxinas bacterianas do intestino para a corrente sanguínea, indicando interrupção na função da barreira intestinal e potenciais efeitos sistêmicos da disbiose.
· Doenças Metabólicas: a inflamação crônica de baixo grau está associada a distúrbios metabólicos, como obesidade e diabetes tipo 2. O LPS das bactérias intestinais pode desencadear a liberação de citocinas pró-inflamatórias, levando à resistência à insulina e à inflamação sistêmica.
· Doença hepática gordurosa não alcoólica (DHGNA): É caracterizada pelo acúmulo de gordura no fígado, frequentemente associada à obesidade e à síndrome metabólica. O aumento da permeabilidade intestinal permite que o LPS entre no fígado, onde ativa as células do sistema imunológico e desencadeia uma resposta inflamatória, levando à inflamação do fígado e à progressão da doença.
· Doença Renal Crônica (DRC): Na DRC, existe um estado de inflamação crônica que contribui para a progressão dos danos renais. O aumento da permeabilidade intestinal e a disbiose intestinal podem resultar na translocação de LPS, desencadeando uma resposta imunológica e promovendo inflamação nos rins.
· Neuroinflamação: A inflamação crônica no sistema nervoso central (SNC) está associada a vários distúrbios neurológicos, incluindo doença de Alzheimer, doença de Parkinson e esclerose múltipla. Estudos indicam que o LPS pode desencadear uma resposta imune no cérebro, levando à produção de citocinas pró-inflamatórias e danos neuronais.



A Doença Celíaca (DC) pode apresentar diferentes sinais. Portanto, de acordo com as diretrizes atuais, os pacientes com sintomas gastrointestinais (má absorção dominada por diarreia, esteatorreia, perda de peso ou atraso no crescimento em crianças), certas doenças (por exemplo, síndrome do intestino irritável, colite microscópica), bem como condições extraintestinais (por exemplo, anemia, sintomas da síndrome do intestino irritável, esofagite de refluxo, neuropatia, ataxia, depressão, osteomalácia e osteoporose, transaminite hepática inexplicada, resultados adversos na gravidez e até mesmo linfoma ou hemossiderose pulmonar) devem ser testados para doença celíaca.
Além disso, pacientes que são parentes de primeiro grau de um celíaco, bem como pacientes com síndromes genéticas (síndrome de Down, Turner-Williams-Beuren e deficiência de IgA) ou doenças autoimunes (diabetes tipo 1, tireoidite autoimune) correm o risco de desenvolver doença celíaca e devem ser testados regularmente.

Contudo, a sua produção excessiva no sangue pode ser sintoma de feocromocitoma, neuroblastoma e, ocasionalmente, de outros tumores neuroectodérmicos.
A serotonina é um neurotransmissor produzido a nível gastrointestinal, envolvido principalmente no ciclo sono/vigília, fome/saciedade, motilidade intestinal, humor, memória e libido. É também considerada a molécula que regula o bom humor e por isso também é conhecida como “hormônio da felicidade”.
A falta de serotonina leva à fibromialgia, doença caracterizada por dores e tensão muscular perene, na origem da rigidez e dificuldade de movimentos. Em vez disso, um excesso de serotonina leva à síndrome da serotonina, caracterizada por dor de cabeça, agitação, confusão, tremores, espasmos musculares, calafrios, taquicardia, sudorese, náusea e diarréia.
A L-DOPA é o precursor da Dopamina, a partir da qual todas as outras Aminas Biogênicas são produzidas através da atividade enzimática do organismo. Também é administrado para atenuar os efeitos da doença de Parkinson, pois esta doença leva a uma diminuição progressiva da produção de dopamina devido à degradação dos neurônios presentes na “substantia nigra”.
As metanefrinas são metabólitos da adrenalina e noradrenalina, sendo produzidas durante o processo de quebra dessas catecolaminas. Elas são liberadas na corrente sanguínea e podem ser medidas para avaliar a atividade do sistema simpático. O aumento nos níveis de metanefrinas pode indicar a presença de tumores neuroendócrinos, como feocromocitoma ou neuroblastoma, semelhante ao que ocorre com as catecolaminas.

A administração de contraste iodado em exames de imagem como tomografia computadorizada (TC) e ressonância magnética (RM) é uma ferramenta essencial para o diagnóstico preciso de diversas doenças. No entanto, o uso de contraste pode levar à nefropatia induzida por contraste (NIC) , uma condição que pode resultar em disfunção renal aguda, especialmente em pacientes com função renal pré-existente comprometida.
A dosagem de creatinina antes da administração de contraste é um procedimento fundamental para avaliar a função renal e identificar pacientes em risco de NIC. A creatinina é um produto residual do metabolismo muscular que é excretado pelos rins, e sua concentração no sangue pode ser utilizada para estimar a taxa de filtração glomerular (TFG), um indicador da função renal .

Neste artigo, exploraremos a carga alostática, seus principais biomarcadores e como eles podem ser utilizados para avaliar o impacto do estresse na saúde.
O que é Carga Alostática?
A carga alostática representa o custo cumulativo das adaptações do organismo a estressores físicos, emocionais e ambientais. Em outras palavras, é a quantidade de energia necessária para o corpo manter o equilíbrio em face de diversos desafios. Quando essa carga se torna cronicamente elevada, pode levar a uma série de problemas de saúde, como distúrbios cardiovasculares, metabólicos e psicológicos.
Bruce McEwen, popularizou a palavra “alostase” para designar a tentativa do corpo de manter um equilíbrio interno diante de circunstâncias instáveis. A palavra combina os gregos állos (variável) e stásis (estase ou paralização) que juntas produzem algo como “permanecer estático em meio à mudança”. Não podemos prescindir disso e nosso corpo fará um grande esforço para manter esse estado, a ponto de causar desgaste a longo prazo se os estresses não cederem.
Biomarcadores associados à uma alta Carga Alostática
Este desgaste nos mecanismos regulatórios do corpo, que McEwen chama de “carga alostática”, causam uma liberação excessiva e prolongada de, principalmente, Adrenalina (neurotransmissor catecolaminérgico) e o hormônio Cortisol (indicador de exaustão do eixo HPA- Hipotalamo-Pituitária-Adrenal). Esses efeitos fisiológicos no corpo podem causar transtornos mentais, doenças autoimunes e a exaustão do próprio aparato do estresse conectados aos centros emocionais do nosso cérebro e fisiológicos de nosso corpo.
Alguns parâmetros que podem ser utilizados para mensurar a carga alostática:
· Biomarcadores Primários - Correlação imediata com a Função Adrenal:
1. Cortisol
Conhecido como o hormônio do estresse, o cortisol é liberado pelas glândulas suprarrenais em resposta ao estímulo do hormônio adrenocorticotrófico (ACTH). Níveis elevados de cortisol são frequentemente associados a uma carga alostática crônica relacionada à exaustão do eixo HPA.
- Produtos disponíveis: Teste Rápido Quantitativo
ou ELISA (soro, plasma, urina ou saliva)
2. Desidroepiandrosterona (DHEA)
DHEA é frequentemente considerado um hormônio antiestresse devido à sua capacidade de modular a resposta do corpo ao estresse. Ele atua como um antagonista do cortisol, o hormônio do estresse, ajudando a equilibrar os efeitos negativos do cortisol sobre o corpo;
- Produtos disponíveis: ELISA (soro, plasma ou saliva)
3. Adrenalina (Epinefrina) e Noradrenalina (Norepinefrina)
Esses hormônios, que também são considerados neurotransmissores, são liberados quando há estímulo no sistema nervoso simpático em resposta ao estresse agudo. Em situações de estresse prolongado, a liberação contínua desses hormônios pode contribuir para a carga alostática.
- Produtos disponíveis: ELISA (plasma, urina ou dried urine spot)
· Biomarcadores Secundários:
1. BNDF - Fator Neurotrófico derivado do cérebro
O BDNF desempenha um papel crucial na saúde cerebral e na regulação do humor. A carga alostática crônica pode influenciar negativamente os níveis de BDNF, uma vez que o estresse prolongado tem sido associado a alterações no sistema nervoso central, afetando a neuroplasticidade e a função cognitiva.
2. Colesterol
A carga alostática pode afetar os níveis de colesterol de várias maneiras. O estresse crônico pode contribuir para mudanças nos hábitos alimentares, aumentar a produção de colesterol pelas glândulas suprarrenais e afetar negativamente o perfil lipídico, aumentando o risco de doenças cardiovasculares.
- Produtos disponíveis: Teste Rápido Quantitativo de Perfil Lipídico
3. Hemoglobina Glicada (HbA1c)
A relação entre carga alostática e HbA1c está relacionada ao estresse crônico e seus efeitos sobre o metabolismo. O estresse prolongado pode influenciar a regulação glicêmica, levando a alterações nos níveis de glicose no sangue ao longo do tempo, refletindo-se na HbA1c.
- Produtos disponíveis: Teste Rápido Quantitativo de HbA1c
4. Proteína C Reativa (PCR) e Interleucina 6 (IL-6) – Biomarcadores de Inflamação
A carga alostática, especialmente quando associada a estresse crônico, pode desencadear respostas inflamatórias persistentes, elevando os níveis de PCR e IL-6, e indicando um estado inflamatório sistêmico.
- Produtos disponíveis: Teste Rápido Quantitativo de PCR Ultrassensível e de Interleucina 6
, Interleucina 6 ELISA
, e PCR Ultrassensível ELISA em Dried Blood Spot
5. Insulina
A resposta ao estresse pode influenciar a sensibilidade à insulina, contribuindo para desregulações metabólicas em situações de carga alostática.
- Produtos disponíveis: Teste Rápido Quantitativo
e ELISA
6. Dopamina
A dopamina é um neurotransmissor envolvido na regulação do prazer, motivação e recompensa. Níveis desregulados podem influenciar a resposta ao estresse.
- Produtos disponíveis: ELISA (plasma, urina ou dried urine spot)
7. GABA (Ácido gama-aminobutírico)
GABA é um neurotransmissor inibitório que desempenha um papel importante na redução da atividade neural. Alterações nos níveis de GABA podem afetar a resposta ao estresse e a regulação emocional.
- Produtos disponíveis: ELISA (plasma, soro, urina ou dried urine spot)
8. Glutamato
Enquanto o GABA é inibitório, o glutamato é excitatório. Níveis alterados de glutamato podem estar associados a respostas exacerbadas ao estresse.
- Produtos disponíveis: ELISA (plasma, soro, urina ou dried urine spot)
Parâmetros Auxiliares:
- Aferição da pressão arterial sistólica e diastólica
- Índice de massa corporal (IMC)
- Relação cintura-quadril.
Situações que podem levar ao aumento de Carga Alóstatica
- Exposição a estressores frequentes que pode determinar um estado de estresse crônico e repetir excitação fisiológica aumentada;
- Falta de adaptação aos estressores;
- Incapacidade de desligar a resposta ao estresse após o término de um estressor;
- Resposta alostática não suficiente para lidar com o estressor.
Em resposta às exigências ambientais, diferentes sistemas fisiológicos interagem em vários graus de atividades. Os sistemas neuroendócrino e imunológico reagem aos desafios internos ou externos e promover adaptação as ameaças ou adversidades.
A carga alostática reflete o efeito acumulativo de experiências da vida diária que envolvem os eventos cotidianos (situações de vida sutis e duradouras) bem como os grandes desafios (eventos de vida), e inclui as consequências fisiológicas da saúde resultante de comportamentos prejudiciais, como sono insatisfatório e ruptura das doenças circadianas, falta de exercício, tabagismo, consumo de álcool e dieta pouco saudável. Quando os desafios ambientais excederem a capacidade individual de lidar com a situação, então a carga alostática segue como uma transição para um estado extremo onde sistemas de resposta ao estresse são repetidamente ativados e fatores padrões de equilíbrio não são adequados.
Conclusão
A relação entre carga alostática e biomarcadores destaca a interconexão complexa entre estresse crônico e saúde. Esses biomarcadores refletem as respostas adaptativas do corpo a uma carga alostática persistente, proporcionando insights importantes para a compreensão dos impactos do estresse prolongado na saúde geral.
Gerenciar a carga alostática pode ser fundamental para preservar a saúde e prevenir condições associadas ao estresse crônico. Estratégias como a adoção de estilos de vida saudáveis, práticas de redução de estresse e apoio psicossocial podem desempenhar um papel crucial na mitigação desses efeitos.
Referências
MacEwen, S. Bruce- The End of Stress as we know it – Dana Press – New York – 2002
Maté, Gabor- O mito do Normal- Trauma, saúde e cura em mundo doente – Editora Sextante – 2023
Allostatic Load and Its Impact on Health: A Systematic Review - Jenny Guidi, Marcella Lucente, Nicoletta Sonino , Giovanni A. Fava - Psychother Psychosom 2021;90:11–27 DOI: 10.1159/000510696

Resumo
O estroboloma, definido como a comunidade de genes bacterianos entéricos capazes de metabolizar estrogênios, emerge como um fator crucial na saúde hormonal. Este artigo revisa a relação entre o estroboloma e a saúde hormonal em diferentes contextos, incluindo:
-
Metabolismo do estrogênio: O estroboloma modula a reabsorção, excreção e biotransformação do estrogênio, impactando seu nível e atividade biológica.
-
Desequilíbrios hormonais: Disfunções no estroboloma podem contribuir para distúrbios como SOP, endometriose e menopausa, afetando a saúde reprodutiva e geral das mulheres.
-
Doenças hormônio-dependentes: O estroboloma pode influenciar o risco e a progressão de doenças como câncer de mama, endometriose e câncer de próstata.
-
Fatores que influenciam o estroboloma: Dieta, antibióticos, estresse e estilo de vida impactam a composição e a atividade do estroboloma.
-
Intervenções para modular o estroboloma: Probióticos, prebióticos, moduladores seletivos do receptor de estrogênio e mudanças no estilo de vida podem ser usados para otimizar a saúde hormonal.

O intricado equilíbrio do sistema endócrino é vital para a homeostase do corpo humano. No entanto, a saturação de carreadores hormonais surge como um fenômeno desafiador, especialmente quando associado ao excesso de produção hormonal. Neste artigo, aprofundaremos os mecanismos subjacentes a esse processo, exploraremos as terapias hormonais e discutiremos a importância da dosagem hormonal na saliva como uma ferramenta diagnóstica crucial.
Mecanismos da Saturação de Carreadores Hormonais
A saturação de carreadores hormonais ocorre quando a produção hormonal ultrapassa a capacidade de transporte dos carreadores disponíveis na corrente sanguínea. Diversos fatores podem desencadear esse fenômeno, como hiperatividade glandular, resistência hormonal nos tecidos-alvo e interferência de substâncias que competem pelos mesmos carreadores.
Excesso de Produção Hormonal
Um dos principais catalisadores da saturação de carreadores é o excesso de produção hormonal por glândulas endócrinas. Este desequilíbrio pode resultar de condições como tumores hipofisários, disfunções da tireoide ou síndrome dos ovários policísticos, desencadeando uma cascata de eventos que leva à sobrecarga dos carreadores hormonais.
Terapias Hormonais e Excesso de Hormônios Exógenos
O uso de doses excessivas de hormônios exógenos durante a terapia hormonal pode sobrecarregar os carreadores hormonais disponíveis no organismo.
Essa sobrecarga pode resultar em uma saturação dos carreadores, já que há uma quantidade maior de hormônios circulantes do que os carreadores podem efetivamente transportar.
A administração regular de hormônios também pode influenciar os padrões naturais de secreção hormonal, levando a uma produção endógena inadequada ou desequilibrada. Essas alterações podem contribuir para a saturação dos carreadores, pois o organismo pode não ser capaz de ajustar adequadamente sua capacidade de transporte.
Resistência nos Tecidos-Alvo
A resistência nos tecidos-alvo refere-se à diminuição da resposta celular a um determinado hormônio, mesmo quando a concentração desse hormônio no sangue está dentro da faixa normal. Isso geralmente ocorre quando há uma disfunção nos receptores hormonais nas células-alvo, impedindo-as de responder adequadamente ao sinal hormonal.
Importância da Dosagem Hormonal na Saliva
A avaliação hormonal tradicionalmente empregou amostras de sangue, mas a dosagem hormonal na saliva está emergindo como uma alternativa valiosa. Este método oferece vantagens, permitindo uma avaliação mais precisa dos níveis hormonais livres, uma vez que a saliva reflete diretamente a fração biologicamente ativa dos hormônios. Além disso, a coleta de saliva é não invasiva e pode fornecer uma visão mais dinâmica dos padrões hormonais ao longo do tempo.
Conclusão
A saturação de carreadores hormonais é um fenômeno complexo que demanda uma abordagem abrangente. Compreender os mecanismos subjacentes, aplicar terapias hormonais específicas e integrar a dosagem hormonal na saliva como uma ferramenta diagnóstica são passos essenciais para tratar eficazmente esse desequilíbrio hormonal.
- Estresse Crônico Prolongado
- Homeostase – Resposta Adaptativa
↑ Pico Matutino (Começou – 4am) - 8:00am - ↓ Sensibilidade Celular
↓ Pico Vespertino 16:00am - ↑ Sensibilidade Celular
↑ Armazenamento de Lipídeos nas Células
↓ Glicogênio – ↑ Glicose
Hipocortisolismo – Mitocôndria – Fadiga Adrenal
Hipercortisolismo – HPA AXIS

A intolerância histamínica é uma condição em que o corpo tem dificuldade em processar adequadamente a histamina, uma substância química naturalmente presente no organismo. A histamina é liberada durante processos alérgicos e desempenha um papel importante em várias funções do corpo, incluindo a regulação do sistema imunológico, a digestão e a regulação do sono.
A intolerância histamínica está associada a uma deficiência ou disfunção de enzimas envolvidas no processo de metabolização da histamina, o que leva ao acúmulo de histamina no corpo. A enzima mais comumente relacionada a esse processo é a diamina oxidase (DAO), que é responsável por quebrar a histamina nos alimentos que consumimos, e também na histamina produzida pelo corpo.
Quando há uma deficiência funcional da DAO, a histamina não é decomposta adequadamente e pode se acumular nos tecidos, levando a uma série de sintomas que são característicos da intolerância histamínica. Este acúmulo de histamina pode ocorrer tanto devido à ingestão de alimentos ricos em histamina quanto à produção endógena de histamina pelo corpo.
É importante notar que a intolerância histamínica não é uma alergia à histamina, mas sim uma reação ao acúmulo excessivo de histamina. As alergias são respostas imunológicas específicas a substâncias estranhas, enquanto a intolerância histamínica envolve uma dificuldade em processar a histamina que está naturalmente presente no corpo e em muitos alimentos.
Os sintomas da intolerância histamínica podem variar amplamente e incluem:
· Problemas gastrointestinais: Dor abdominal, inchaço, flatulência, diarreia ou constipação;
· Sintomas cutâneos: Coceira, urticária, erupções cutâneas e vermelhidão;
· Sintomas respiratórios: Coriza, congestão nasal, espirros, tosse e dificuldade respiratória;
· Sintomas neurológicos: Dores de cabeça, enxaquecas, tontura, fadiga e confusão mental;
· Sintomas cardíacos: Palpitação e hipotensão (pressão arterial baixa);
· Outros sintomas: Ansiedade, insônia, cólicas menstruais e dores musculares.
O diagnóstico da intolerância histamínica pode ser um desafio, uma vez que os sintomas se assemelham a muitas outras condições. Geralmente, um diagnóstico é feito com base na avaliação clínica, obtendo informações sobre seus sintomas, histórico médico, hábitos alimentares e outros fatores relevantes para avaliar a possibilidade de intolerância histamínica. Os testes laboratoriais, como medir os níveis de histamina e DAO no sangue, ajuda a avaliar se há um desequilíbrio entre a produção de histamina e sua metabolização, contribuindo para a avaliação diagnóstica e o uso de um planejamento alimentar, bem como a eliminação temporária de alimentos ricos em histamina.
Portanto, o tratamento da intolerância histamínica envolve evitar alimentos ricos em histamina e adotar uma dieta de baixa histamina. Além disso, alguns profissionais de saúde podem recomendar a suplementação de enzimas DAO para ajudar na metabolização da histamina, medicamentos anti-histamínicos também podem ser usados para aliviar os sintomas, bloqueando os efeitos da histamina no corpo e proporcionando alívio temporário.
Conheça nossa linha de Intolerância Histamínica:
· Histamina ELISA (Amostra urina e
plasma)
· Histamina ELISA (Amostra sangue
total)
·
Histamina ELISA (Fezes)
O Clostridium difficile é uma bactéria anaeróbica que pode causar infecções intestinais graves, especialmente em pessoas com sistema imunológico enfraquecido ou após o uso prolongado de antibióticos. Essa infecção pode levar à colite pseudomembranosa, uma inflamação grave do cólon que pode ser fatal.
A microbiota intestinal, também conhecida como flora intestinal, é composta por bilhões de micro-organismos, incluindo bactérias, vírus e fungos, que vivem no trato gastrointestinal. Esses micro-organismos desempenham um papel crucial na digestão, absorção de nutrientes e regulação do sistema imunológico.
Uma microbiota intestinal saudável é diversa e equilibrada, com uma ampla variedade de bactérias benéficas, como Bifidobacterium e Lactobacillus. Além destes, algumas cepas de Clostridium podem ajudar a manter o equilíbrio da microbiota intestinal, produzindo ácidos graxos de cadeia curta, que são importantes para o funcionamento saudável do cólon. Além disso, essas bactérias podem ajudar a regular o sistema imunológico, reduzindo a inflamação intestinal.
No entanto, outras cepas de Clostridium, como Clostridium difficile , podem ser patogênicas e causar infecções no intestino, incluindo colite pseudomembranosa. Essas cepas nocivas geralmente se tornam mais comuns em situações em que a microbiota intestinal é prejudicada, como após o uso prolongado de antibióticos.
O Clostridium difficile produz toxinas que danificam a mucosa intestinal e causam inflamação, diarreia, cólicas e dor abdominal. A infecção por C. difficile é responsável por cerca de 20% dos casos de diarreia associada a antibióticos e pode levar a complicações graves, incluindo desidratação, insuficiência renal e septicemia.
Além do uso excessivo de antibióticos, outros fatores que aumentam o risco de infecção por C. difficile incluem idade avançada, internação hospitalar, procedimentos cirúrgicos, doenças crônicas e uso prolongado de medicamentos que suprimem o sistema imunológico.
Portanto, a relação entre Clostridium e a saúde da microbiota intestinal é complexa e depende das espécies específicas presentes na microbiota. É importante manter um equilíbrio saudável da microbiota intestinal para evitar o crescimento excessivo de espécies potencialmente patogênicas, incluindo o Clostridium difficile.
Referências:
Seekatz, A. M., & Young, V. B. (2014). Clostridium difficile and the microbiota. Journal of clinical investigation, 124(10), 4182-4189. https://doi.org/10.1172/JCI72336
Kelly, C. P., & LaMont, J. T. (2008). Clostridium difficile—more difficult than ever. New England Journal of Medicine, 359(18), 1932-1940. https://doi.org/10.1056/NEJMra0707500
Leffler, D. A., & Lamont, J. T. (2015). Clostridium difficile infection. New England Journal of Medicine, 372(16), 1539-1548. https://doi.org/10.1056/NEJMra1403772
Cohen, S. H., Gerding, D. N., Johnson, S., Kelly, C. P., Loo, V. G., McDonald, L. C., ... & Wilcox, M. H. (2010). Clinical practice guidelines for Clostridium difficile infection in adults: 2010 update by the society for healthcare epidemiology of America (SHEA) and the infectious diseases society of America (IDSA). Infection control and hospital epidemiology, 31(5), 431-455. https://doi.org/10.1086/651706
Debast, S. B., Bauer, M. P., Kuijper, E. J., & European Society of Clinical Microbiology and Infectious Diseases. (2014). European Society of Clinical Microbiology and Infectious Diseases: update of the treatment guidance document for Clostridium difficile infection. Clinical Microbiology and Infection, 20(suppl_2), 1-26. https://doi.org/10.1111/1469-0691.12418

O que é Autismo?
O autismo é um transtorno do desenvolvimento que afeta a comunicação, interação social e comportamento. Embora a causa exata do autismo ainda não seja conhecida, vários fatores têm sido associados a ele, incluindo fatores genéticos, ambientais e imunológicos. Recentemente, tem havido interesse crescente na relação entre o autismo e a zonulina.
O que é Zonulina?
A zonulina é uma proteína que regula a permeabilidade intestinal. Ela é produzida no intestino e ajuda a controlar a abertura das junções entre as células intestinais, permitindo a passagem de nutrientes e outras substâncias para o corpo. Quando há um aumento da produção de zonulina, a permeabilidade intestinal pode ser aumentada, permitindo que substâncias indesejadas entrem na corrente sanguínea. Isso é conhecido como "intestino permeável".
Relação entre Zonulina e Autismo
Há evidências de que pessoas com autismo têm uma maior incidência de problemas gastrointestinais, incluindo o intestino permeável. Um estudo publicado na revista científica Molecular Autism em 2013, encontrou níveis significativamente mais elevados de zonulina em crianças com autismo em comparação com crianças sem autismo.
Além disso, pesquisas têm demonstrado que a zonulina pode ter um efeito sobre o sistema imunológico, aumentando a permeabilidade das células cerebrais e permitindo a passagem de substâncias tóxicas para o cérebro. Essa permeabilidade pode levar a inflamação e danos neuronais, que têm sido associados a doenças neuropsiquiátricas, incluindo o autismo.
Estudos recentes sugerem que o aumento da zonulina no intestino pode levar à formação de autoanticorpos que afetam o funcionamento do cérebro e podem estar associados ao desenvolvimento do autismo. Esses autoanticorpos podem atacar proteínas cerebrais, levando a danos neuronais e à manifestação de sintomas do autismo.
Níveis elevados de zonulina podem estar relacionados a disfunções na produção de hormônios e neurotransmissores no cérebro, incluindo a ocitocina, um hormônio associado à sociabilidade e ao comportamento afetivo. A redução na produção de ocitocina pode estar relacionada a dificuldades sociais e de comunicação observadas em indivíduos com autismo.
Conheça nossa linha de testes para medicina Integrativa e Funcional
Aumento no número de casos de autismo nos últimos 20 anos
Desde a década de 1990, tem havido um aumento significativo no número de casos de autismo em todo o mundo. Nos Estados Unidos, por exemplo, a taxa de prevalência do autismo em crianças de 8 anos aumentou de cerca de 1 em 150 crianças em 2000, para cerca de 1 em cada 44 crianças em 2018 e 1 em 36 crianças em 2020, de acordo com o Centro de Controle e Prevenção de Doenças (CDC). Essa tendência também é observada em muitos outros países, incluindo o Brasil.
Uma das razões para o aumento no número de casos de autismo é o maior reconhecimento e diagnóstico do transtorno. Nos últimos anos, houve um maior conhecimento e conscientização sobre o autismo, levando a um maior número de diagnósticos em crianças e adultos. Além disso, os critérios de diagnóstico para o autismo têm sido ampliados e aprimorados, o que pode ter contribuído para o aumento do número de casos diagnosticados.
Outro fator que pode estar contribuindo para o aumento no número de casos de autismo é a mudança nos estilos de vida e no ambiente em que as pessoas vivem. Por exemplo, a exposição a poluentes ambientais, como produtos químicos tóxicos, pode estar afetando o desenvolvimento fetal e aumentando o risco de transtornos do desenvolvimento, incluindo o autismo. Além disso, mudanças na dieta, incluindo o aumento do consumo de alimentos processados e a redução da ingestão de nutrientes importantes, podem estar afetando o desenvolvimento infantil.
Por fim, os fatores genéticos também podem estar contribuindo para o aumento no número de casos de autismo. Pesquisas indicam que o autismo é altamente hereditário, o que significa que pode haver uma predisposição genética para o transtorno. No entanto, a genética sozinha não pode explicar o aumento significativo no número de casos de autismo observado nas últimas décadas.
O aumento no número de casos de autismo tem implicações significativas para a sociedade, incluindo um aumento na demanda por serviços de saúde e educação especial. Além disso, o autismo pode ter um impacto negativo na qualidade de vida dos indivíduos afetados e de suas famílias, levando a desafios sociais, emocionais e financeiros.
Referências
Fasano, A. (2012). Zonulin and its regulation of intestinal barrier function: the biological door to inflammation, autoimmunity, and cancer. Physiological reviews, 91(1), 151-175.
Fiorentino, M., Sapone, A., Senger, S., Camhi, S. S., Kadzielski, S. M., Buie, T. M., & Fasano, A. (2016). Blood-brain barrier and intestinal epithelial barrier alterations in autism spectrum disorders. Molecular autism, 7(1), 49.
de Magistris, L., Familiari, V., Pascotto, A., Sapone, A., Frolli, A., Iardino, P., ... & Bravaccio, C. (2010). Alterations of the intestinal barrier in patients with autism spectrum disorders and in their first-degree relatives. Journal of pediatric gastroenterology and nutrition, 51(4), 418-424.
Fiorentino, M., Franchi, E., Pascotto, A., & Fasano, A. (2013). Zonulin upregulation is associated with increased gut permeability in subjects with type 1 diabetes and their relatives. Diabetes, 62(12), 3926-3930.
Russo, R., Murzilli, S., Pellegrini, F., & Lopetuso, L. R. (2018). Inflammatory bowel disease and autism spectrum disorders: searching for a connection. Inflammatory bowel diseases, 24(4), 674-683.
Johnson, C. P., & Myers, S. M. (2007). Identification and evaluation of children with autism spectrum disorders. Pediatrics, 120(5), 1183-1215.
Waly, M. I., Hornig, M., Trivedi, M., Hodgson, N., Kini, R., Ohta, A., ... & Fasano, A. (2016). P1-031: Evidence of zonulin secretion in children with autism spectrum disorders. Clinical and experimental immunology, 184(S1), 174-174.
Baio, J., Wiggins, L., Christensen, D. L., Maenner, M. J., Daniels, J., Warren, Z., ... & Dowling, N. F. (2018). Prevalence of autism spectrum disorder among children aged 8 years—autism and developmental disabilities monitoring network, 11 sites, United States, 2014. MMWR Surveillance Summaries, 67(6), 1-23.
Hertz-Picciotto, I., Croen, L. A., Hansen, R., Jones, C. R., van de Water, J., & Pessah, I. N. (2018). The rise in autism and the role of age at diagnosis. Epidemiology, 29(5), 689-696.
Lyall, K., Croen, L. A., Daniels, J. L., Fallin, M. D., Ladd-Acosta, C., Lee, B. K., ... & Volk, H. E. (2017). The changing epidemiology of autism spectrum disorders. Annual Review of Public Health, 38, 81-102.
Newschaffer, C. J., Croen, L. A., Daniels, J., Giarelli, E., Grether, J. K., Levy, S. E., ... & Yoon, P. W. (2007). The epidemiology of autism spectrum disorders. Annual Review of Public Health, 28, 235-258.
Sandin, S., Lichtenstein, P., Kuja-Halkola, R., Larsson, H., Hultman, C. M., & Reichenberg, A. (2017). The familial risk of autism. JAMA, 318(4), 393-395.

A dosagem de neurotransmissores na urina é uma técnica utilizada para avaliar a presença e quantidade de substâncias químicas responsáveis pela comunicação entre as células nervosas no corpo humano. Essas substâncias, conhecidas como neurotransmissores, incluem serotonina, dopamina, noradrenalina e ácido gama-aminobutírico (GABA), entre outros.A dosagem de neurotransmissores na urina pode ser realizada por meio de exames laboratoriais, que avaliam a concentração dessas substâncias na amostra de urina coletada. Esses exames podem ser úteis na avaliação de distúrbios neurológicos e psiquiátricos, como depressão, ansiedade e transtornos de déficit de atenção e hiperatividade (TDAH).
Como funciona?A técnica de dosagem de neurotransmissores na urina envolve a coleta da urina em um recipiente estéril, seguida da análise laboratorial dos níveis de neurotransmissores presentes na amostra. A interpretação dos resultados deve ser feita por um profissional capacitado, levando em consideração o histórico clínico e os sintomas do paciente.
Em resumo, a dosagem de neurotransmissores na urina é uma técnica útil para avaliar a atividade do sistema nervoso e pode auxiliar no diagnóstico e no monitoramento do tratamento de diversas condições clínicas.
Quais as vantagens?
Existem algumas vantagens da dosagem de neurotransmissores na urina em relação à dosagem no sangue:
1. Coleta mais fácil: a coleta de urina é geralmente mais fácil e menos invasiva do que a coleta de sangue, o que pode tornar o processo mais confortável para o paciente.
2. Maior estabilidade dos neurotransmissores: os neurotransmissores presentes na urina são geralmente mais estáveis do que os presentes no sangue, o que pode aumentar a precisão dos resultados.
3. Menor interferência de fatores externos: os níveis de neurotransmissores na urina são menos suscetíveis a flutuações causadas por fatores externos, como a alimentação e o estresse emocional, do que os níveis no sangue.
4. Mais específico para avaliar a atividade neuronal: a urina reflete mais diretamente a atividade neuronal do que o sangue, uma vez que os neurotransmissores na urina são derivados do sistema nervoso central e não de outras fontes no corpo.
Quais são os testes de neurotransmissores na urina disponíveis?
• Serotonina
• GABA
• Dopamina
• Epinefrina
• Noraepinefrina
• Triptofano
• Glutamato
Entre em contato conosco para saber mais.
Conclusão
Em resumo, a dosagem de neurotransmissores na urina é uma técnica útil para avaliar a atividade do sistema nervoso e pode auxiliar no diagnóstico e no monitoramento do tratamento de diversas condições clínicas.
Referências
Kim YK, Lee HP, Won SD, et al. Low plasma GABA levels and the correlation with the alpha EEG in medication-naive patients with depression: a pilot study. Prog Neuropsychopharmacol Biol Psychiatry. 2007;31(1):78-85.
Mijatovic T, Jovanovic M, Gavrilovic L, et al. Urinary neurotransmitter testing: assessing the activity of the autonomic nervous system. Adv Clin Chem. 2019;90:197-238.
Bongiovanni R, Carpaneto E, Canepa E, et al. A review of the clinical uses and analytical methods for urine neurotransmitter testing. Clin Chem Lab Med. 2017;55(11):1610-1621.
Gupta S, Masand PS, Kaplan D, et al. The use of urinary neurotransmitter testing to identify patients with depression at risk for suicide. Ann Clin Psychiatry. 2016;28(1):31-41.

· O que é a Doença Celíaca?
A doença celíaca ou sensibilidade ao glúten é caracterizada por danos no intestino delgado levando a uma chamada mucosa “plana”. Devido a essas lesões extensas, a má absorção ocorre frequentemente acompanhada de uma depleção de nutrientes essenciais. A fração solúvel em álcool do glúten, a gliadina, substrato da transglutaminase tecidual (tTG), representa um agente causador da doença celíaca, por estimular um processo inflamatório no intestino delgado. As respostas imunes celular e humoral são provavelmente desencadeadas pela ligação cruzada da gliadina em complexos moleculares elevados. O método sorológico de diagnóstico da doença celíaca inclui a detecção de anticorpos IgA e IgG para transglutaminase tecidual (Anti-tTg IgA/IgG) e gliadina desamidada (GliaDea IgA/IgG) . Os anticorpos IgA para a transglutaminase tecidual são considerados de maior valor preditivo, portanto, os pacientes que sofrem de deficiência de IgA, uma doença concomitante frequente em pacientes celíacos, podem ser diagnosticados com anticorpos do tipo IgG.
O diagnóstico da doença celíaca e da dermatite herpetiforme compreende a biópsia do intestino delgado demonstrando uma mucosa “plana” antes de uma dieta sem glúten e a seguinte reconstituição da mucosa após o início da dieta. A determinação de IgG e IgA para gliadina desamidada por ELISA, bem como a detecção de autoantígenos endomisiais humanos (EmA) IgA tem sido considerada como os principais parâmetros sorológicos para doença celíaca até agora.
O diabetes tipo 2 pode levar anos para se desenvolver e, se detectado precocemente, é uma doença totalmente evitável. Um novo estudo sugere que um biomarcador sanguíneo específico pode ser usado para identificar esses pacientes a caminho de um diagnóstico de diabetes, mas ainda para exibir sintomas da doença.
Atualmente, os médicos que realizam exames de saúde de rotina geralmente medem os níveis de açúcar no sangue de um paciente. Quando esses níveis de açúcar no sangue estão elevados, mas abaixo do limite oficial para diabetes tipo 2, pode-se diagnosticar uma condição chamada pré-diabetes.
No entanto, nem todos os pacientes com pré-diabetes irão desenvolver diabetes tipo 2. De fato, apenas cerca de 50% das pessoas com pré-diabetes progredirão para diabetes em um acompanhamento de 10 anos. Então, além do rastreamento de glicose no sangue, como os médicos podem identificar os pacientes mais próximos do desenvolvimento clínico de diabetes tipo 2?
Uma das principais características patológicas do diabetes é o comprometimento da secreção de insulina pelas células beta do pâncreas. À medida que o diabetes tipo 2 progride, essas células beta tornam-se cada vez mais danificadas e, no momento em que a doença é claramente diagnosticável, os pacientes tendem a ter perdido cerca de metade dessas células cruciais.
Identificar a transição do pré-diabetes para o diabetes é complexo, pois o estado das células afetadas, que estão espalhadas em quantidades muito pequenas no núcleo de um órgão localizado sob o fígado, o pâncreas, é impossível de avaliar quantitativamente por métodos não invasivos. investigações”, explicou Pierre Maechler, pesquisador principal do novo estudo. “Optamos, então, por uma estratégia alternativa: encontrar uma molécula cujos níveis no sangue estariam associados à massa funcional dessas células beta para detectar indiretamente sua alteração na fase de pré-diabetes, antes do aparecimento de qualquer sintoma. ”
Então, em vez de rastrear o pré-diabetes simplesmente observando os níveis de glicose no sangue, Maechler partiu para encontrar um biomarcador
E neste estudo recém-publicado, os pesquisadores relatam que o biomarcador realmente se correlaciona com o diabetes em humanos. Em várias análises diferentes, o estudo demonstrou que baixos níveis de 1,5-anidroglucitol podem estar associados a déficits nas células beta pancreáticas.
O estudo primeiro mostrou que os diabéticos têm níveis sanguíneos mais baixos de 1,5-anidroglucitol em comparação com os não diabéticos. Mas talvez o mais interessante é que os pesquisadores confirmaram a ligação entre o 1,5-anidroglucitol e as células beta estudando as mudanças nos níveis sanguíneos em pacientes submetidos à cirurgia para remover partes do pâncreas.
“O diabetes é uma doença complexa em que muitas alterações metabólicas ocorrem em paralelo”, disse Maechler.
“Era, portanto, essencial testar a relevância desse marcador em pessoas que sofrem uma perda repentina de suas células beta, mas na ausência de distúrbios metabólicos. Ao estudar o nível de 1,5-anidroglucitol em indivíduos cuja metade do pâncreas foi removida cirurgicamente, pudemos demonstrar que o 1,5-anidroglucitol é um indicador sanguíneo da quantidade funcional das células beta pancreáticas.”
GlycoMark® – Diagnóstico Laboratorial de 1,5 anidroglucitol – kit Registrado na Anvisa pela ArgosLab Distribuidora de Produtos para Laboratório Ltda.
RALEIGH, NC, 16 de novembro de 2021 - Precision Diabetes, Inc. anuncia hoje a apresentação de dados que demonstram que o teste de 1,5-anidroglucitol (GlycoMark®) é mais preciso do que os testes comumente usados, hemoglobina A1c (HbA1c) e glicose, em predizer mortalidade em pacientes com COVID-19 hospitalizados com e sem diabetes. O estudo, “1,5-anidroglucitol é um preditor independente de mortalidade em pacientes com COVID-19”, foi apresentado na conferência American Heart Association (AHA) 2021 Scientific Sessions.
O estudo, conduzido no Sinai Hospital em Baltimore, Maryland, mostrou que o teste GlycoMark® tinha 76% de precisão de mortalidade (AUC) em comparação com a precisão de HbA1c e glicose de jejum de 51% e 60%, respectivamente. Curiosamente, a precisão do GlycoMark® foi maior em pacientes sem diabetes (79%) do que em pacientes com diabetes (73%). Um algoritmo, que incluiu idade, IMC e GlycoMark®, teve uma precisão de predição de mortalidade de 89%.
“Ficamos satisfeitos em descobrir que o teste GlycoMark® identificou a mortalidade com alta precisão em pacientes COVID-19, disse Paul Gurbel, MD, cardiologista do The LifeBridge Health Cardiovascular Institute e investigador principal do estudo. GlycoMark® pode ter utilidade na triagem de pacientes COVID-19 em ambiente hospitalar com maior risco de gravidade e mortalidade. Isso pode ser especialmente importante em pacientes não diabéticos COVID-19 que podem desenvolver diabetes de início recente, o que traz maiores riscos de doença grave e morte.”
Este estudo segue um estudo relatado anteriormente apresentado como um resumo de última hora nas sessões científicas da American Diabetes Association (ADA) de 2021, que mostrou que GlycoMark® foi um marcador eficaz de hiperglicemia de estresse e gravidade em pacientes com COVID-19, particularmente em pacientes sem diabetes. O estudo foi realizado no Hospital Universitario Cruces em Bilbao, Espanha.
O Kit GlycoMark® está Registrado na ANVISA sob número 80464810727 através da ArgosLab®.

O coronavírus contém quatro proteínas estruturais, incluindo proteínas de spike (S), envelope (E), membrana (M) e nucleocapsídeo (N). Entre eles, a proteína S desempenha os papéis mais importantes na fixação, fusão e entrada viral, e serve como um alvo para o desenvolvimento de anticorpos, inibidores de entrada e vacinas.
A proteína S permite a entrada viral nas células hospedeiras ligando-se primeiro a um receptor hospedeiro através do domínio de ligação ao receptor (RBD) na subunidade S1 e, em seguida, fundindo as membranas viral e hospedeira através da subunidade S2.
As vacinas SARS-CoV-2 baseadas em mRNA são seguras e eficazes. As vacinas provocam respostas de anticorpos contra o RBD (o principal alvo dos anticorpos neutralizantes) de uma maneira que se assemelha à infecção natural.
De acordo com o artigo publicado na Revista Nature de Fevereiro de 2021, as Vacinas de mRNA foram capazes a partir de oito semanas após a segunda dose, em voluntários, apresentarem níveis elevados de título de proteína de pico IgM e de IgG anti Spike -SARS-CoV-2 (S) e (anti RBD).
“mRNA vaccine-elicited antibodies toSARS-CoV-2 and circulating variants-“ - Zijun Wang et al - NATURE, February 2021.
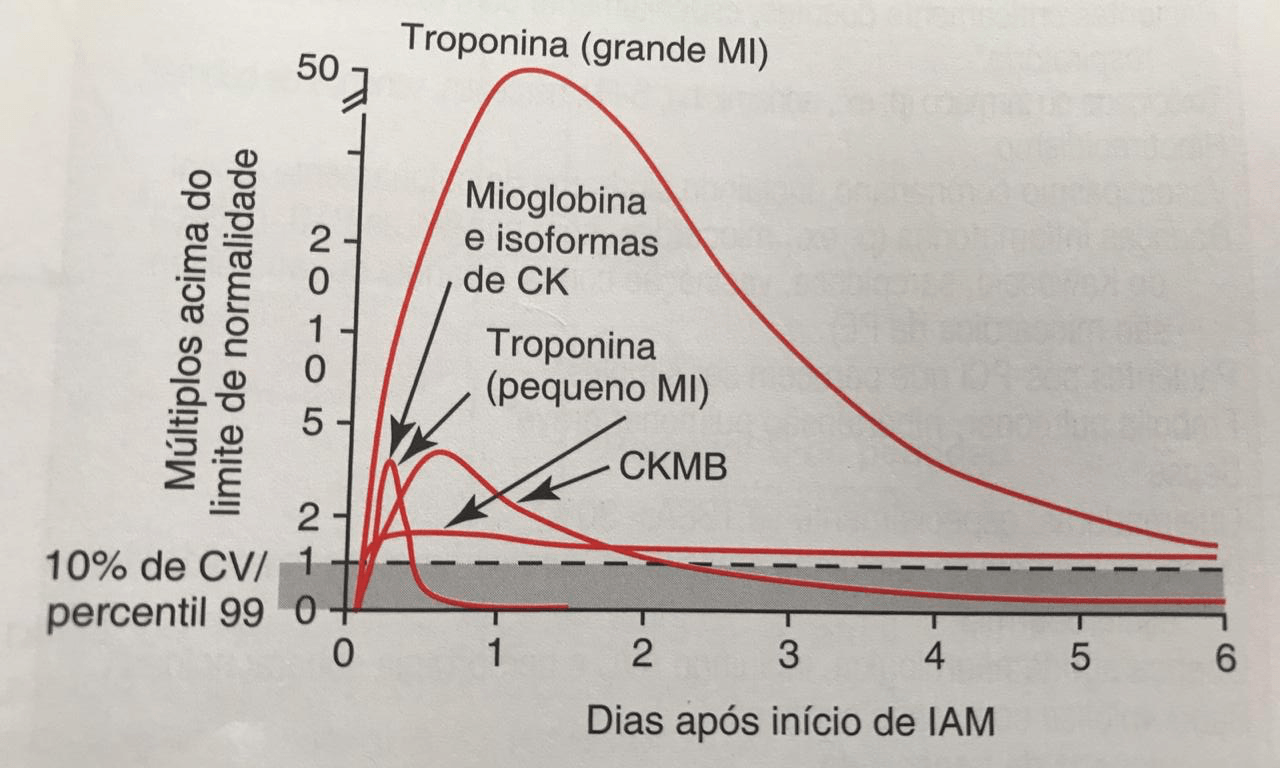
A padronização dos ensaios de cTn permanece indefinida. O subcomitê de padronização de cTnI da American Association for Clinical Chemistry (AACC), em colaboração com o National Institute od Standards and Technology (NIST), tem produzido um material de referência padrão para cTnI (SRM # 2921), que é um complexo TnC-cTnI-cTnT purificado a partir do coração humano sob condições não denaturantes. Uma vez que foi descoberto que este material é comutável com apenas 50% de ensaios de cTnI atuais, ele passou a ter um valor limitado para a harmonização de ensaios nos testes atuais e não é útil como um calibrador comum. Isso, no entanto, permite a rastreabilidade para um material de referência comum. Atualmente, um Grupo de Trabalho da International Federation of Clinical Chemistry and Laboratory Medicine (IFCC) está trabalhando para desenvolver um material de referência secundário baseado em soro.
Em 2001, o Comitê sobre Padronização de Marcadores de Lesão Cardíaca (C-SMCD) do IFCC atualizou as especificações de qualidade para ensaios de cTn destinadas aos fabricantes de ensaios comerciais e aos laboratórios clínicos que utilizam análises de cTn. O Objetivo geral foi uma tentativa de estabelecer critérios uniformes de modo que todos os ensaios poderiam ser avaliados objetivamente por suas qualidades analíticas e performance clínica.

